Што е тераностика?
Тераностика е термин за комбинација на терапевтски и дијагностички средства (користење на еден радионуклид за сликање на тумори и втор радионуклид за лекување на тумори со доставување зрачење што го убива ракот). Во основа, тоа значи таргетирање на единствена рецепторска молекула на клетките на ракот со два различни радионуклиди (слика и терапија). Ова е за да се постигне прецизна и персонализирана стратегија за третман.
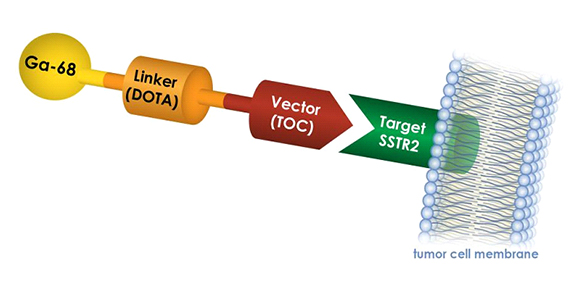
Дијагностичка фаза на Тераностикс
Туморските клетки имаат обвивка, наречена мембрана; постојат одредени протеини како што е соматостатин рецепторот (SSTR2) на клеточната мембрана на туморот кои можат да послужат како цел за лекови за рак.
Ga-68 DOTATOC е радиоактивен дијагностички лек кој го таргетира SSTR2. Ga-68 DOTATOC се инјектира во вената на пациентот и патува низ крвотокот до сите органи и ткива на телото. Ако пациентот има невроендокрин тумор со SSTR2 на клеточните мембрани на туморот, Ga-68 DOTATOC ќе се поврзе со SSTR2 и туморот ќе светне на ПЕТ скен
Терапевтската фаза на Theranostics
Откако ќе се дијагностицира невроендокриниот карцином со помош на Ga68-DOTATOC PET скен, Ga-68 може да се замени со друг радионуклид, како што е лутециум-177 (Lu-177) или итриум-90 (Y-90), кој може да ги таргетира и убие клетките на туморот кои имаат SSTR2 на нивните мембрани.
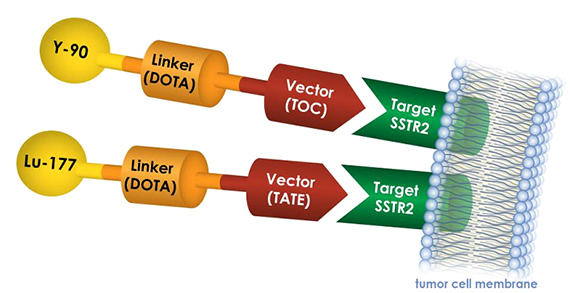
Терапевтските Y-90-DOTATOC и Lu-177-DOTATATE може да се инјектираат во вените на пациентот и да патуваат до кој било дел од телото што има SSTR2 протеини. Овие терапевтски лекови се врзуваат за SSTR2 протеините како клуч во бравата, дозволувајќи му на лекот да влезе во клетките на туморот и да го убие со оштетување на ДНК на таа клетка. Здравите клетки околу туморот кои немаат SSTR2 протеини на нивната мембрана не се засегнати од лекот.
Таквата стратегија им овозможува на онколозите поцелосно да ги сликаат ткивата на ракот што се лекуваат, да избираат пациенти за терапевтски апликации, да видат прецизно каде ќе се доставуваат терапевтските агенси и да ја следат способноста на терапевтскиот агенс да ги намалува туморите со текот на времето. Theranostics им обезбедува на онколозите нови и високо ефективни алатки за да креираат прецизни стратегии за третман и да ги предвидат придобивките од одреден третман врз основа на уникатниот молекуларен и геномски профил на пациентите.
ТЕРАНОСТИКА: ГЛЕДАЊЕ ШТО ЛЕКУВАМЕ - ЛЕКУВАЊЕ НА ОНА ШТО ГЛЕДАМЕ
Ова е исто така наречено насочена радионуклидна терапија бидејќи е насочен кон одредената молекуларна цел на функционалните клетки на ракот. Затоа, поголема доза на зрачење може да биде насочена кон туморот без да влијае на многу нормални здрави клетки.
Како тераностиката се разликува од традиционалната радиотерапија?
Терапијата со зрачење може да биде многу ефикасна во лекувањето на ракот или да ги ублажи симптомите кај пациенти со неизлечиви карциноми во напредна фаза. Приближно половина од сите пациенти со рак ќе добијат терапија со зрачење во одреден момент од нивниот третман, која користи надворешно или внатрешно испорачани рендгенски зраци, протони или други честички со висока енергија за да ги таргетира и уништи клетките на ракот. Додека подобрените технолошки пристапи го намалија влошувањето на здравото ткиво, традиционалната радиотерапија сè уште предизвикува несакани ефекти кои може да биде тешко да се толерираат за некои пациенти. Покрај тоа, традиционалната радиотерапија не е во состојба да таргетира повеќе од една локација на болеста, ограничувајќи ја нејзината корисност за пациенти со метастатски карцином. Сепак, традиционалната радиотерапија останува една од најмоќните алатки за третман на онкологијата.
Овој нов пристап кон третманот на туморот - насочена радионуклидна терапија - ја реинженеринг употребата на третмани со зрачење во прецизната онкологија и дава нова класа на терапии за рак. Целта на развојот на насочена радионуклидна терапија е да се комбинираат изотопи кои емитуваат алфа-, бета- или гама-честички - или радионуклиди - со пептиди, антитела или мали молекули, за да се развијат терапии со висока специфичност за одредени типови на тумори. Доставени до пациентот интравенски, насочените радионуклиди терапии се дизајнирани да патуваат директно до туморот за да доставуваат терапевтско зрачење со висока прецизност. Оваа прецизност е наменета за фокусирање на испораката на зрачењето до туморското ткиво додека ја минимизира изложеноста на радијација на нормалното ткиво.
Каков вид на рак може да се лекува со тераностици?
Тераностиците можат да бидат ефикасни во лекувањето на метастатски, неоперабилни тумори во напредната фаза на болеста, вклучувајќи рак на простата, невроендокрини тумори на различни органи како желудникот, панкреасот, тенкото и дебелото црево и белите дробови. Последно, но не и најмалку важно, постоперативната аблација на резидуалниот остаток на тироидната жлезда и третманот на метастатски карцином на тироидната жлезда е исто така во опсегот на тераностиците.
Горенаведените видови на рак имаат доволно докази достапни во моментов дека постои дефинитивна корист од користењето на радионуклидна терапија. Сепак, многу други видови на рак исто така може да имаат корист кога изразуваат одредени типови на целни рецептори како што се протеинот за активирање на фибробластите (FAP) и рецепторите на хемокин (CXCR4), кои можат да бидат насочени со тераностици.
Нашите молекуларни и насочени радионуклиди тераностици вклучуваат:
-
- PRRT: Лутециум -177 DOTA терапија
Актиниум – 225 DOTA терапија
Итриум-90 DOTA терапија за невроендокрини тумори - PRLT: Лутециум -177 PSMA терапија за рак на простата
- ТАРЕ: Терапија со сфера со итриум-90 SIR за рак на црниот дроб / метастази на црниот дроб
- FAPI: Активирање на фибробластите Терапија со протеински инхибитор
Лутециум-177 ФАПИ терапија и
Actinium -225 FAPI Терапија за околу 28 типови напредни карциноми
- PRRT: Лутециум -177 DOTA терапија
- Исто така: Добро позната I – 131 Радио-јод терапија за карциноми на тироидната жлездаСамариум – 153 Палијативна терапија на болка за коскени метастази. I-131 MIBG терапија за феохромоцитом
Досега се разгледува само на исклучителни клинички сценарија на сочувствителна основа.
Преземете го летокот


Победа над Ракот со Центарот за рак на Аполо Протон
Пробив во грижата за ракот! Глобалниот растечки товар од рак раскажува застрашувачка приказна. За да се спротивстави на оваа растечка закана, Центарот за рак на Apollo Proton обезбедува целосно и сеопфатно решение. Бидејќи грижата за ракот стана еден од најбрзо растечките императиви за здравствена заштита ширум светот, веруваме дека е од клучно значење да ја редефинираме нашата цел, да ја рестартираме нашата посветеност на едноумниот фокус - да се бориме со ракот, да го победиме ракот!

Авторски права © 2026 Аполо протон центар за рак. Сите права се задржани





